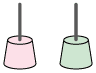|
|
|
준비물 |
|
|
실험과 관찰 |
1.
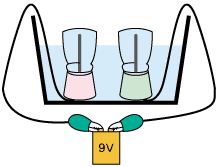
준비된 2 개의 야구르트 컵의 중앙에 구멍을 내고 연필심을
꽂는다.
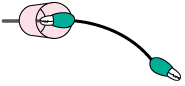
2.
꽂힌 안 쪽의 연필심에 전기선을 꽂는다.
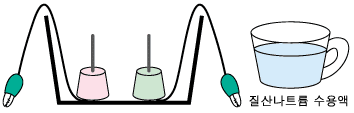
3.
수조에 연필심이 꽂힌 두 개의 컵을 넣고 질산나트륨을 완전히
녹인 용액을 붓는다.
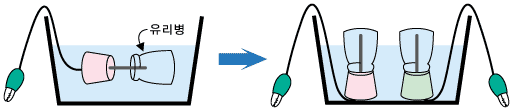
4. 수조 안에서 유리병을 잠기도록 하여 야구르트 컵과 유리병을 물로 가득 채워 공기가 들어가지 않도록 하고 연필심이 꽂힌 컵을 서서히 기울여서 연필심이 유리병 속에 들어가도록 한다.
5.
연필심이 꽂힌 컵과 유리병을 똑바로 세운 다음 두
전선을 9 V를 전지 +극과 -극에 각각 연결시켜 전류를
흐르게 한다.
6. 어떤 현상이 일어나는지 관찰해 보자. |
|
|
|
|
|
|
|
▲ 실험 시작한지 30분 후 |
|
▲ 실험 시작한지 60분 후 |
||
|
왜 그럴까요? |
물은 물 분자 라는 것이 엄청나게 많이 모여 있는 것입니다. 그리고 물 분자 하나는 수소 원자 2 개와 산소 원자 1 개로 이루어져 있지요.
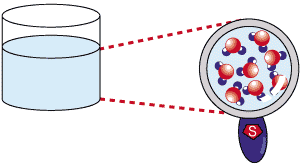

아래는 산소 원자, 수소 원자, 물 분자를 표현하기 위해 흔히 사용하는 모형입니다.
|
|
|
|
|
|
|
|
▲ 산소 원자 |
|
▲ 수소 원자 |
|
▲ 물 분자 |
|
로케트를 위로 올려보내기 위해서는 많은 에너지가 순간적으로 필요한데, 이때 사용되는 연료가 수소 기체입니다. 수소 기체를 산소 기체로 태우면 엄청난 양의 열이 생기거든요. 그리고 물이 생깁니다.입니다.

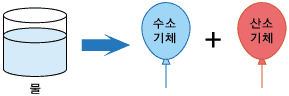
이번 실험에서 한 물의 분해는 물을 수소 기체와 산소 기체로 바꾸어 주는 것을 말합니다. 위의 과정의 반대입니다.
<물의 분해>
|
|
수소 기체와 산소 기체가 물로 변하는 과정에서 열(에너지)이 밖으로 나오므로, 물이 수소 기체와 산소 기체로 되기 위해서는 에너지가 들어가야겠지요. 이 실험에서는 물이 수소 기체와 산소 기체로 분해되기 위해 필요한 에너지로 전지의 전기 에너지를 사용하였습니다. 그래서 물의 전기 분해라고 합니다.
<물의 전기 분해>
|
|
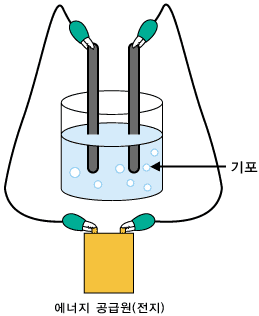
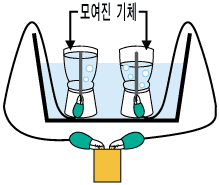
위의 그림에서와 같이 전지의 +극과 -극에 전선으로 연결된 연필심(흑연)을 물에 담그면, 연필심 주위에서 기포가 뽀글뽀글 생기는 것을 관찰할 수 있습니다. 이것이 바로 수소 기체와 산소 기체입니다. 수소 기체는 한 연필심 주변에서 생기고, 산소 기체는 다른 연필심 주위에서 생깁니다.
이렇게 물이 전기 분해되어 생기는 수소 기체와 산소 기체는 두 유리병 안에 따로 모을 수 있습니다. 바로 이번 실험에서 한 것이지요.
|
|
눈을 크게 뜨고 자세히 보니 이상한 점을 발견했어요. 유리병에 모인 두 기체의 부피가 다르네요. |
|
|
물이 분해되어 생기는 수소 기체와 산소 기체의 부피는 다르답니다. 이것을 이해하려면 화학 반응을 이해해야 합니다. 화학 반응은 원자들이 짝을 바꾸는 과정입니다. 화학 반응 도중 원자는 없어지지도 생기지도 않아요. 물 분자를 이루는 원 수소 원자와 산소 원자가 수소 기체를 이루는 수소 분자와 산소 기체를 이루는 산소 분자로 변해가는 과정은 다음과 같습니다. |
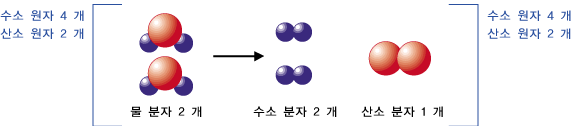
위의 그림에서 알 수 있듯이 물이 전기 분해되면 산소 분자 1 개 생길 때마다 수소 분자는 2 개씩 생기지요. 기체의 부피는 기체를 이루는 기체 분자의 수에 비례합니다. 기체 분자 수가 2배면, 기체의 부피도 2배가 됩니다. 따라서 수소 기체의 부피는 산소 기체의 부피의 2 배입니다