|
▶ 산성/염기성 수용액과 금속의 반응 |
|
산성 수용액에 철과 마그네슘을 담그면 어떤 일이 일어날까요? 아래 동영상에서 확인해보세요.
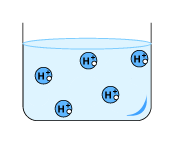
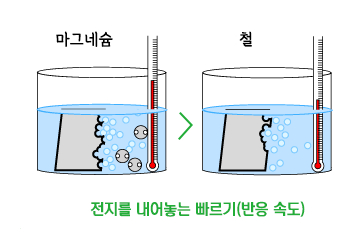
철과 마그네슘을 염산과 황산 수용액에 넣으면 기포가 발생합니다. 철과 마그네슘을 비교하면, 철에 비해 마그네슘을 산에 넣었을 때 더 많은 기포가 발생합니다. 마그네슘의 경우 온도도 많이 올라갑니다. 반면, 철의 경우에는 온도가 거의 변하지 않거나 조금 올라갑니다.
기포가 발생한다는 것은 기체 상태의 새로운 물질이 생겼다는 것을 알려줍니다. 즉, 철이나 마그네숨은 산성 수용액과 반응한다는 것입니다. 철과 마그네슘을 비교하면, 철에 비해 마그네슘이 산성 수용액과 더 빨리 반응한다는 것을 알 수 있습니다. 온도는 열이 들어왔을 때 올라갑니다. 따라서 마그네슘이 산성 수용액과 반응할 때에는 많은 열이 발생한다는 것을 알 수 있습니다.(더 자세한 것은 페이지 맨 아래 깊이 알기 참조)
염기성 수용액에 철과 마그네슘을 담그면 어떤 일이 일어날까요? 아래 동영상에서 확인해보세요.
수산화나트륨 수용액 속에서 철과 마그네슘에는 아무 변화가 관찰되지 않습니다. 온도 또한 변하지 않습니다.
이것으로부터 철이나 마그네숨은 염기성 수용액과 반응하지 않는다는 것을 알 수 있습니다..
|

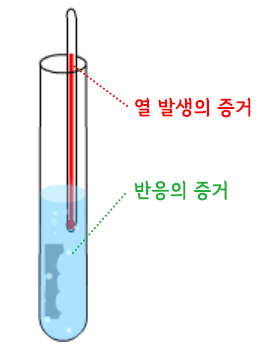

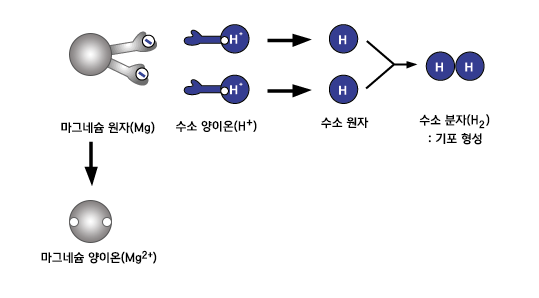
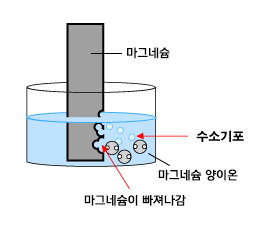
 마그네슘과 철이 산성 수용액과 반응하면?
마그네슘과 철이 산성 수용액과 반응하면?