|
▶ 산화와 환원(Ⅱ): 전자의 이동과 산화-환원 |
|
산성 수용액에 철과 마그네슘을 담그면 어떤 일이 일어날까요? 아래 동영상에서 확인해보세요.
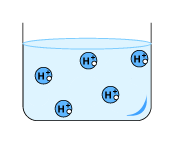
철과 마그네슘을 염산과 황산 수용액에 넣으면 기포가 발생합니다. 철과 마그네슘을 비교하면, 철에 비해 마그네슘을 산에 넣었을 때 더 많은 기포가 발생합니다. 마그네슘의 경우 온도도 많이 올라갑니다. 반면, 철의 경우에는 온도가 거의 변하지 않거나 조금 올라갑니다.
염산과 황산 수용액에는 공통적으로 수소 양이온(H+)이 들어 있습니다.
철과 마그네슘은 각각 철원자와 마그네슘 원자로 이루어져 있습니다.
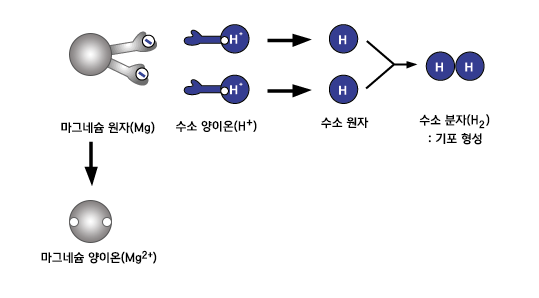
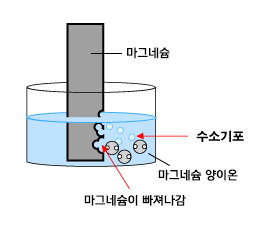
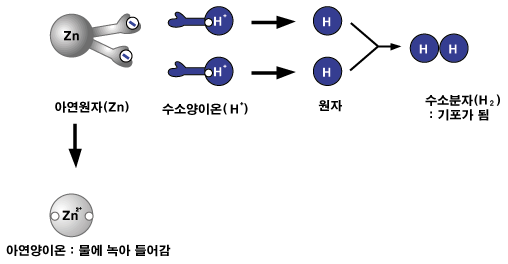
철이나 마그네슘 원자들은 수소 양이온을 만나면 가지고 있던 전자들을 아주 잘 내어 줍니다. 전자를 내어준 금속들은 양이온이 됩니다. 이 양이온들은 물 속으로 녹아들어 가지요. 전자를 받은 수소 양이온은 어떻게 되냐구요? 2개의 수소 양이온이 전자를 받은 후 수소 분자가 됩니다. 수소 분자들이 아주아주 많이 모인 것이 수소 기체입니다. 물 속에서 생긴 수소는 기포(기체 주머니)가 되어 뽀글뽀글 날아가지요.
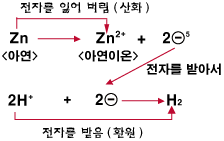
아연도 산성 수용액에 넣으면, 아연 원자들은 전자 2개를 잃고 아연 양이온이 됩니다. 이 전자들을 수수 양이온이 받아 수소 분자가 되지요.
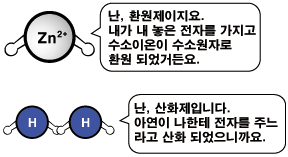
이렇게 전자를 잃거나 얻는 반응도 산화-환원 반응입니다. 전자를 잃으면 '산화되었다'고 하고 전자를 얻으면 '환원되었다'고 합니다. 산화와 환원은 항상 동시에 일어납니다. 왜냐하면 누군가 전자를 내어놓으면 그것을 다른 누군가가 받아야 하니까요.
이 반응에서 아연이 전자를 내놓아서 수소를 환원시킨 것이지요. 이렇게 전자를 내어놓고 산화되는 물질은 다른 물질을 환원시키는 물질을 환원제라고 합니다. 반대로 환원되는 물질은 다른 물질을 산화시키므로 산화제라고 합니다.
옷의 얼룩을 없애주는 것 중에 산화표백제라는 것이 있습니다. 그것이 옷의 얼룩을 제거하는 과정도 산화-환원 반응입니다.
|